Изотерма. Изобара. Изохора. Газовые законы
Изопроцесс - процесс, при котором один из макроскопических параметров состояния газа данной массы остается постоянным.
Изотермической процесс - процесс изменения состояния газа определенной массы при постоянной температуре.
Закон Бойля-Мариотта: для газа данной массы при постоянной температуре $$ p_{1}V_{1}=p_{2}V_{2} $$ , где - $ p_{1} $,$ p_{2} $ давление и $ V_{1} $,$ V_{2} $ объём газа в начальном и конечном состояниях.
Изотерма - график изменения макроскопических параметров газа при изотермическом процессе.
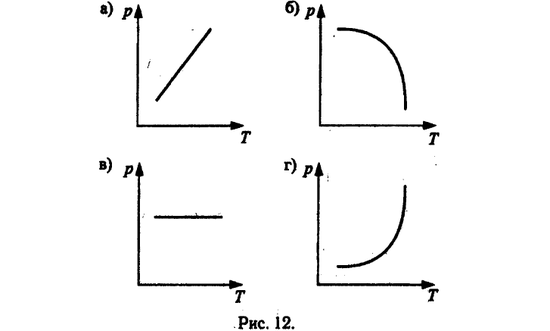
Изобарный процесс - процесс изменения состояния газа определенной массы при постоянном давлении. Рис 12. в)
Закон Гей-Люссака: для газа данной массы при постоянном давлении $$ \frac{V_{1}}{T_{1}}=\frac{V_{2}}{T_{2}} $$ где- ${V_{1}}$,${V_{2}}$,${T_{1}}$,${T_{2}}$ - объем и температура газа в начальном и конечном состояниях.
Изобара - график изменения макроскопических параметров газа при изобарном процессе.
Изохорный процесс – процесс изменения состояния газа определенной массы при постоянном объеме. (V=const. m=const) Рис 12. а)
Закон Шарля: для газа данной массы при постоянном объеме $$ \frac{p_{1}}{T_{1}}=\frac{p_{2}}{T_{2}} $$ где $ {p_{1}} $,$ p_{2} $,${T_{1}}$,${T_{2}}$ -давление и температура газа в начальном и конечном состояниях.
Изохора - график изменения макроскопических параметров газа при изохорном процессе.
Закон Дальтона для давления смеси газов $$ p= p_{1}+p_{2}+\ldots+p_{n} $$ n - число газов,
$ p_{i} $ - порпорциональное давление i-го газа (i=1,2,….,n), т.е. давление, которое оказывал бы стенку сосуда i-ый газ при отсутствии других газов.
Задачи и опыты
Задачи
Изотерма. изобара. изохора. Газовые законы. Задача 1
Изотерма. изобара. изохора. Газовые законы. Задача 2